Danno da emotrasfusione: presupposti e limiti dell’azione di risarcimento

1.
L’espressione danno da sangue infetto designa qualsivoglia pregiudizio derivante da contagio di patologie mediante trasfusione di sangue o somministrazione di emoderivati.
L’azione di risarcimento dei danni da emotrasfusioni o emoderivati trae origine, nella maggioranza dei casi, da un fatto dannoso che colpisce il soggetto che, per una sua patologia congenita, è costretto con periodicità, in tutto l’arco della sua vita, a sottoporsi a emotrasfusioni e ad assumere emoderivati, presso una o più strutture sanitarie. In un minor numero di casi il contagio avviene, invece, in conseguenza di un singolo fatto traumatico, per esempio, l’operazione chirurgica, il parto o l’infortunio che rendono necessaria una trasfusione.
Nella prima serie di casi è particolarmente complesso individuare con precisione quale sia stata la singola trasfusione o la somministrazione di prodotti che abbia causato la contrazione del virus e in certi casi anche presso quale struttura sia avvenuto il contagio. Di conseguenza, i soggetti danneggiati, nella maggior parte dei casi, preferiscono indirizzare l’azione verso il Ministero della salute, facendo valere la loro responsabilità per i danni causati dalla violazione dei doveri di sorveglianza e di controllo che su di esso gravano quale principale responsabile della raccolta e distribuzione del sangue, nonché della prevenzione dei rischi. In taluni casi, alla ipotizzata responsabilità del Ministero si affianca quella, di natura contrattuale, del medico o dell’ospedale.
Nella seconda serie di casi, invece, in cui le patologie sono contratte da un soggetto a seguito di un singolo fatto potenzialmente dannoso, l’unicità dell’assunzione del prodotto a rischio spinge spesso il danneggiato a indirizzare l’azione direttamente nei confronti del soggetto o della struttura che ritiene responsabile del suo contagio.
È evidente che dall’impostazione della causa come volta a far valere la responsabilità contrattuale o extracontrattuale del convenuto discendono rilevanti differenze in ordine a molteplici profili, quali il termine, decennale o quinquennale, di prescrizione dell’azione, la decorrenza del suddetto termine di prescrizione, il contenuto dell’onere probatorio in relazione al nesso causale e alla responsabilità colposa o dolosa del convenuto, l’ampiezza dell’area del danno risarcibile.
2. Il termine di prescrizione dell’azione risarcitoria
Importante sotto tale profilo è la questione relativa al termine di prescrizione dell’azione risarcitoria e al dies a quo da cui tale azione decorre.
In tema di responsabilità extracontrattuale del Ministero della Salute per i danni da trasfusione di sangue infetto, in caso di decesso del danneggiato a causa del contagio, la prescrizione rimane quinquennale per il danno subito da quel soggetto in vita, del quale il congiunto chieda il risarcimento iure hereditatis, trattandosi di un danno da lesione colposa, soggetto a prescrizione quinquennale dalla data del fatto.
La prescrizione è, invece, decennale per il danno subito dai congiunti della vittima iure proprio, in quanto, per tale aspetto, il decesso del congiunto emotrasfuso integra omicidio colposo, reato a prescrizione decennale (cfr. Cass. Civ. n. 28464/2013; Cass.Civ.n.7553/2012).
Il termine di prescrizione del diritto al risarcimento del danno da parte di chi assume di avere contratto per contagio da emotrasfusioni una malattia per fatto doloso o colposo di un terzo decorre dal giorno in cui tale malattia venga percepita – o possa essere percepita usando l’ordinaria diligenza e tenendo conto della diffusione delle conoscenze scientifiche – quale danno ingiusto conseguente al comportamento del terzo, con la precisazione che la presentazione della domanda di indennizzo di cui alla legge n. 210 del 1992 segna solo il limite temporale ultimo di possibile decorrenza del termine di prescrizione, senza che ciò escluda la possibilità di collocare l’effettiva conoscenza della rapportabilità causale della malattia in un momento precedente, tenendo conto delle informazioni in possesso del danneggiato e della diffusione delle conoscenze scientifiche, in base a un accertamento che è rimesso al giudice del merito (cfr. Cass. civ. n. 23635/2015; Cass. Civ. n. 10551/2015; Cass Civ. n. 10530/2015). In caso di patologie conseguenti a infezione da virus HBV, HIV e HCV, contratte a seguito di emotrasfusioni o di somministrazione di emoderivati, sussiste la responsabilità del Ministero della Salute anche per le trasfusioni eseguite in epoca anteriore alla conoscenza scientifica di tali virus e all’apprestamento dei relativi test identificativi (risalenti, rispettivamente, agli anni a978, 1985, 1988), atteso che già dalla fine degli anni ’60 era noto il rischio di trasmissione di epatite virale ed era possibile la rilevazione (indiretta) del virus, che della stessa costituiscono evoluzione o mutazione, mediante gli indicatori della funzionalità epatica, gravando pertanto sul Ministero della salute, in adempimento degli obblighi specifici di vigilanza e controllo posti da una pluralità di fonti normative speciali risalenti già all’anno 1958, l’obbligo di controllare che il sangue utilizzato per le trasfusioni e gli emoderivati fosse esente da virus e che i donatori non presentassero alterazione della transaminasi (cfr. Cass. Civ. n. 3721/2019; Cass. Civ. n. 1566/2019).
In particolare, il Ministero della Salute, in base a una pluralità di fonti normative (per l’elenco esaustivo delle quali, ex plurimis, Cass. n. 18520/2018), è tenuto a esercitare un ‘attività di controllo e di vigilanza in ordine (anche) alla pratica terapeutica della trasfusione del sangue e dell’uso degli emoderivati, e risponde ex art. 2043 c.c., per omessa vigilanza, dei danni conseguenti a epatite e a infezione da HIV contratte da soggetti emotrasfusi (Cass. Civ. n. 17685/2011; Cass. Civ. n. 9404/2011; Cass. Civ. S.U. n. 584/2008; Cass. Civ. S.U. n. 576/2008).
In tema di danni da emotrasfusioni, nel giudizio promosso dal danneggiato contro il Ministero della salute, l’accertamento della riconducibilità del contagio a una emotrasfusione, compiuto dalla Commissione di cui all’art. 4 della l. n. 210 del 1992, in base al quale è stato riconosciuto l’indennizzo ai sensi di detta legge, non può essere messo in discussione dal Ministero, quanto alla riconducibilità del contagio alla trasfusione o alle trasfusioni individuate come causative di esso, e il giudice deve ritenere detto fatto indiscutibile e non bisognoso di prova, in quanto, essendo la Commissione organo dello Stato, l’accertamento è da ritenere imputabile allo stesso Ministero (Cass. Civ. n. 15734/2018).
In tema di risarcimento da emotrasfusione infetta, la compensatio lucri cum damno tra l’indennizzo corrisposto al danneggiato, ai sensi dell’art. 1 della legge 25 febbraio 1992, n. 210, e il risarcimento richiesto al Ministero della Sanità per l’omessa adozione di adeguate misure di emovigilanza, integra un’eccezione in senso lato, rilevabile d’ufficio e proponibile per la prima volta anche in appello (cfr. Cass. Civ. n. 991/2014).
Nel giudizio promosso nei confronti del Ministero della Salute per il risarcimento del danno conseguente al contagio da virus HBV, HIV o HCV a seguito di emotrasfusioni con sangue infetto, l’indennizzo di cui alla l. n. 210 del 1992 non può essere scomputato dalle somme liquidabili a titolo di risarcimento del danno (compensatio lucri cum damno), qualora l’importo dell’indennizzo non sia stato corrisposto e tantomeno determinato o determinabile, in base agli atti di causa, nel suo preciso ammontare, posto che l’astratta spettanza di una somma suscettibile di essere compresa tra un minimo e un massimo, a seconda della patologia riconosciuta, non equivale alla sua corresponsione e non fornisce elementi per individuarne l’esatto ammontare, né il carattere predeterminato delle tabelle consente di individuare, in mancanza di dati specifici a cui è onerato chi eccepisce il lucrum, il preciso importo da portare in decurtazione del risarcimento (Cass. Civ. n. 2778/2019; Cass. Civ. n. 32944/2018).
Sulla base di ciò, la prescrizione dell’azione risarcitoria decorre dal momento in cui l’emotrasfuso comprende e ricollega, secondo l’ordinaria diligenza e tenuto conto della diffusione delle conoscenze scientifiche dell’epoca, che la sua patologia è stata contratta a seguito di trasfusione.
Se non si conosce la causa del contagio, infatti, la prescrizione non inizia a decorrere, poiché la malattia, sofferta come tragica fatalità non imputabile a un terzo, non è idonea a concretizzare il “fatto” che l’art. 2947, c.1, c.c. individua quale esordio della prescrizione.
Sul punto, le Sezioni Unite hanno chiarito che non può ritenersi che la prescrizione inizi a decorrere solo con la comunicazione del responso della Commissione medica ospedaliera di cui all’art. 4 della legge n. 210/1992; ciò in quanto, dal momento che l’indennizzo, di cui alla citata legge, è dovuto in presenza di danni irreversibili da vaccinazioni, emotrasfusioni o somministrazioni di emoderivati, è ragionevole ritenere che già al momento della proposizione della domanda amministrativa la vittima del contagio abbia acquisito sufficiente percezione della malattia, delle cause e delle conseguenze dannose.
Trattandosi, dunque, di fatto dannoso “lungo-latente”, per il quale può intercorrere un lasso di tempo rilevante tra l’intervento sanitario e il momento in cui la malattia viene (o può) essere percepita, il danneggiato potrà agire a notevole distanza di tempo dall’effettuazione delle emotrasfusioni infette.
Conformi in tal senso le decisioni giurisprudenziali: Cass. civ., Sez. Un., 11 gennaio 2008, n. 577; Cass. civ., sez. III, 14 luglio 2011, n. 15453; Cass. civ., Sez. III, 23 gennaio 2014 n. 1355secondo cui «La responsabilità del Ministero della salute per i danni conseguenti a infezioni da virus HBV, HIV, HCV contratte da soggetti emotrasfusi è di natura extracontrattuale, né sono ipotizzabili, al riguardo, figure di reato tali da innalzare i termini di prescrizione (epidemia colposa o lesioni colpose plurime); ne consegue che il diritto al risarcimento del danno da parte di chi assume di aver contratto tali patologie per fatto doloso o colposo di un terzo è soggetto al termine di prescrizione quinquennale che decorre, a norma degli artt. 2935 e 2947, 1 co. c.c. dal giorno in cui tale malattia viene percepita o può essere percepita quale danno ingiusto conseguente al comportamento del terzo, usando l’ordinaria diligenza e tenendo conto della diffusione delle conoscenze scientifiche».
3. Presumibile responsabilità del ministro della salute
In premessa va chiarito che diversi soggetti potrebbero essere in astratto convenuti per il risarcimento del danno da emoderivati, a partire dal Ministero della salute, su cui gravano obblighi di sorveglianza e controllo, fino ad arrivare alla struttura ospedaliera coinvolta e al medico o ai medici che abbiano effettuato concretamente le operazioni.
Per ciascun soggetto la giurisprudenza ha individuato uno specifico inquadramento di responsabilità legato al ruolo che il medesimo ha svolto nella prevenzione e nell’esclusione del danno da emotrasfusione.
Per quanto attiene al Ministero della salute, gli interpreti inquadrano nell’ambito della responsabilità extracontrattuale ex art. 2043 c.c. la responsabilità per omesso controllo e vigilanza sulle procedure fissate per l’emotrasfusione.
Diversamente, per le case farmaceutiche distributrici di farmaci pericolosi la responsabilità trova il suo inquadramento nell’art. 2050 c.c.
Nel caso delle strutture sanitarie viene invece in rilievo una “responsabilità contrattuale da contatto sociale”.
Pertanto, la responsabilità potrà considerarsi contrattuale nei confronti del medico e della struttura sanitaria con cui il paziente viene in contatto, ma dovrà ritenersi extracontrattuale nei riguardi del Ministero della salute, con tutte le conseguenze in punto di onere della prova e durata dei termini di prescrizione per far valere la relativa azione risarcitoria.
3.1 Indennizzo risarcimento e tabelle
Quando si parla di danno da emotrasfusione è necessario distinguere tra l’indennizzo dovuto in base alla l. 210/1992 e il risarcimento del danno ex art. 2043 cc.
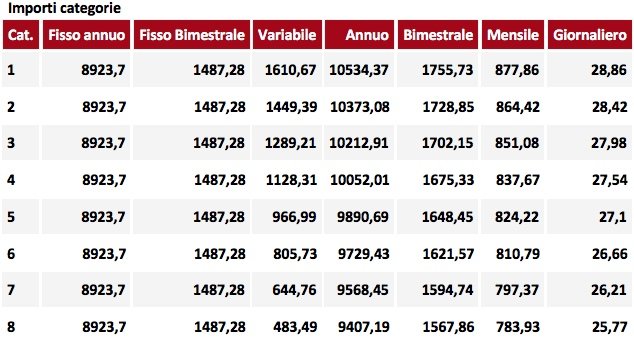
L’indennizzo di cui alla l. n. 210/1992, dovuto dallo Stato, è riconosciuto a coloro i quali presentino danni irreversibili da epatiti post-trasfusionali o da epatite contratta a seguito di somministrazioni di derivati del sangue e consiste in un assegno composto da una somma determinata nella misura stabilita dalla tabella B allegata alla legge 177/76, cumulabile con ogni altro emolumento a qualsiasi titolo percepito e da una somma corrispondente all’importo dell’indennità integrativa speciale di cui alla l. 324/59. Esso si compone quindi di due quote: una prima quota che rappresenta il vero e proprio indennizzo, e una seconda quota che integra la prima, detta appunto indennità integrativa speciale.
Tabella importi indennizzo
L’indennizzo di cui sopra è integrato da una somma corrispondente all’indennità integrativa speciale di cui alla Legge 27 maggio 1959, n. 324 e successive modifiche, prevista per la prima qualifica funzionale degli impiegati civili dello Stato.
Riportiamo di seguito, anno per anno dal 1995 al 2011, gli importi dell’indennizzo ex legge n. 210/1992 corrispondenti a ognuna delle otto categorie della tabella di legge cui è stata ascritta l’infermità riportata a seguito di vaccinazione, trasfusioni di sangue o somministrazione di emoderivati.
4. La responsabilità del Ministero della salute
La responsabilità del Ministero della salute per i danni conseguenti a infezioni da HIV e da epatite contratte da soggetti emotrasfusi per l’omessa vigilanza esercitata dall’Amministrazione sulla sostanza ematica negli interventi trasfusionali e sugli emoderivati è stata inquadrata nella violazione della clausola generale di cui all’art. 2043 c.c.
Al mantenimento di tale condotta di vigilanza, sicurezza e attivo controllo, l’Amministrazione è, d’altro canto, tenuta già in base all’obbligo di buona fede o correttezza, generale principio di solidarietà sociale – che trova applicazione anche in tema di responsabilità extracontrattuale – in base al quale, nei rapporti della vita di relazione, ciascuno è tenuto a mantenere un comportamento leale che si specifica in obblighi di informazione e di avviso, nonché volto alla salvaguardia dell’utilità altrui, nei limiti dell’apprezzabile sacrificio, dalla cui violazione conseguono profili di responsabilità in ordine ai falsi affidamenti anche solo colposamente.
Appare rilevante l’individuazione della responsabilità del Ministero, in quanto il giudizio relativo alla sussistenza del nesso causale non può limitarsi alla mera valutazione della materialità fattuale, bensì postula la preventiva individuazione dell’obbligo specifico o generico di tenere la condotta omessa.
Dato che il giudice è tenuto ad accertare se l’evento sia ricollegabile all’omissione (causalità omissiva), ovvero se esso non si sarebbe verificato qualora (causalità ipotetica) l’agente avesse posto in essere la condotta doverosa impostagli, con esclusione di fattori alternativi, allora l’accertamento del rapporto di causalità ipotetica passa attraverso l’enunciato controfattuale che pone al posto dell’omissione il comportamento alternativo doveroso, onde verificare se esso avrebbe evitato il danno lamentato dal danneggiato. In termini probatori, ciò comporta che il paziente il quale si pretenda danneggiato dall’inadempimento della prestazione di cura ha l’onere di provare il fatto costitutivo del rapporto obbligatorio (legge o contratto) e di allegare un inadempimento efficiente alla produzione del danno.
Si deve, peraltro, notare come la prova del nesso causale tra la specifica trasfusione e il contagio da virus HIV, ove risulti provata l’idoneità di tale condotta a provocarla, può essere fornita anche con il ricorso alle presunzioni (art. 2729 c.c.)
Il primo punctum dolens consiste nella pluralità dei soggetti contro cui è teoricamente esperibile l’azione risarcitoria: – il personale sanitario che ha praticato la trasfusione; – la struttura dove quest’ultima è stata eseguita; – la branca dell’amministrazione centrale investita del compito di vigilare sulla sicurezza del sangue e dei suoi derivati. L’ipotesi meno frequente è, nella prassi, la chiamata in giudizio degli appartenenti al primo gruppo, ciononostante è stata configurata la responsabilità colposa, nonché, in ipotesi limitate, integrante il dolo eventuale, a carico dei medici di un centro trasfusionale che non si astengano dal fornire sangue proveniente da donatori rimasti ignoti e sui quali non sia consentito effettuare alcuna verifica. Rispetto alle altre due categorie di potenziali danneggianti, è opportuno in primo luogo operare una distinzione di fondo sul regime di responsabilità cui possono andare incontro. Con riferimento alle strutture sanitarie, la fattispecie va inquadrata nell’ambito della responsabilità contrattuale, come indicato dalla Cassazione, nelle sentenze n. 9315/2010 e n. 25277/2009. È stata peraltro esclusa, come si rinviene da Cassazione n. 3261/2016, la sussistenza di un inadempimento contrattuale a carico della singola struttura ospedaliera, pubblica o privata, inserita nella rete del Servizio Sanitario Nazionale, che abbia utilizzato sacche di sangue, provenienti dal servizio di immunoematologia trasfusionale dell’Azienda Sanitaria Locale, preventivamente sottoposte ai controlli richiesti dalla normativa dell’epoca. Esula, infatti, in tal caso dalla diligenza esigibile dalla struttura il dovere di conoscere e attuare le misure attestate dalla più alta scienza medica a livello mondiale per evitare la trasmissione del virus, almeno quando essa non provveda direttamente con un autonomo centro trasfusionale. Sussiste, invece, responsabilità extracontrattuale allorquando i danni cagionati dalla trasfusione vengono addebitati al comportamento omissivo del Ministero della Salute. In particolare rilievo è la violazione della clausola generale di cui all’art. 2043 c.c., mentre non si può ricondurre la fattispecie alla responsabilità per l’esercizio di attività pericolose prevista dall’art. 2050 c.c., come statuito dalla Cassazione nella sentenza n. 1136 del 2015. Sempre in questo ambito, la Suprema Corte, con sentenza n. 10291/2015, ha puntualizzato che la condanna del Ministero per contagio da trasfusioni, postula, in primo luogo, il riscontro dell’omissione dell’attività di controllo, di direttiva e di vigilanza, nonché dell’esistenza della patologia e dell’assenza di altri fattori causali alternativi. In secondo luogo, è necessario procedere all’accertamento, avuto riguardo all’epoca di produzione del preparato, della conoscenza oggettiva, ai più alti livelli scientifici, della possibile veicolazione di virus attraverso sangue infetto, sì da far ritenere, secondo un giudizio ipotetico, che l’azione omessa avrebbe potuto impedire l’evento in quanto era obbiettivamente prevedibile che ne sarebbe potuta derivare come conseguenza la lesione. Si è ulteriormente specificato che, pur potendosi risalire ad altra data antecedente, la prova di tale conoscenza deve ritenersi raggiunta a partire dal 1978, anno del riconoscimento del virus dell’epatite B da parte dell’Organizzazione Mondiale della Sanità. Stessa conclusione vale anche per il contagio da HIV e da epatite C, posto che i diversi virus non costituiscono eventi autonomi e diversi, ma solo forme di manifestazioni patogene dello stesso evento lesivo. In particolare, la Cassazione, con ordinanza n. 2232/2016, ha affermato la responsabilità del Ministero per i danni provocati dal contagio dell’epatite C, a seguito di trasfusioni eseguite nel 1974. Con sentenze nn. 10291/2015 e 20933/2015, la Suprema Corte ha invece cassato sia la decisione che aveva sancito la responsabilità del Ministero per i danni provocati dal contagio da epatite C insorta in occasione di trasfusioni eseguite tra il 1970 e il 1974, sia la sentenza d’appello che aveva escluso la responsabilità del Ministero per i danni provocati dal contagio dell’epatite C in occasione di trasfusioni di sangue infetto eseguite nel 1983. Si tenga altresì presente che il Consiglio di Stato, con sentenza n. 2479 del 2015, ha reputato illegittima la disposizione dettata da un decreto ministeriale che restringeva indebitamente l’applicazione dei moduli previsti per le transazioni da stipulare con i soggetti danneggiati da trasfusione con sangue infetto o da somministrazione di emoderivati infetti, limitandone l’utilizzo ai casi in cui l’evento trasfusionale non fosse anteriore al 24 luglio 1978.
In ordine alla responsabilità del Ministero, in giurisprudenza si afferma, inoltre, che, in tema di patologie conseguenti a infezioni con i virus HBV (epatite B), HIV (AIDS) e HCV (epatite C), contratte a causa di assunzione di emotrasfusioni o di emoderivati con sangue infetto, per l’unicità dell’evento lesivo consistente nella lesione dell’integrità fisica, vi è una presunzione di responsabilità del Ministero della salute per il contagio verificatosi negli anni prima del 1979 tra il 1979 e il 1989, stante l’avvenuta scoperta scientifica della prevedibilità delle relative infezioni, individuabile nel 1978, con il conseguente obbligo di controllo e di vigilanza in materia di raccolta e distribuzione di sangue umano per uso terapeutico, presunzione che può essere vinta solo se viene fornita dallo stesso Ministero la prova dell’adozione di condotte e misure necessarie per evitare il contagio, a prescindere dalla conoscenza di strumenti di prevenzione specifica.
In altri termini, il Ministero della salute è tenuto a esercitare un’attività di controllo e di vigilanza sulla pratica terapeutica della trasfusione del sangue e sull’uso degli emoderivati, per cui risponde, ai sensi dell’art. 2043 c.c., dei danni conseguenti a epatite e a infezione da HIV, contratte da soggetti emotrasfusi, per omessa vigilanza sulla sostanza ematica e sugli emoderivati.
Corte di Cassazione, sez. III Civile – Sentenza 20 maggio 2015, n. 10291
«In tema di responsabilità omissiva per contagio (in capo al Ministero), si applica il principio della regolarità causale della condotta omissiva che presuppone, oltre all’accertamento della violazione dell’obbligo di tenere la condotta, l’accertamento, in riferimento all’epoca di produzione del preparato, della conoscenza oggettiva ai più alti livelli scientifici della possibile veicolazione di virus attraverso sangue infetto, in modo che, secondo un giudizio ipotetico, possa dirsi che l’azione omessa avrebbe potuto impedire l’evento, essendo oggettivamente prevedibile che ne sarebbe potuta derivare come conseguenza la lesione. E tale accertamento che – unitamente all’accertamento della omissione dell’attività dovuta, della esistenza della patologia, dell’assenza di altri fattori causali alternativi – rientra nelle competenze del giudice del merito, deve ritenersi raggiunto con il riconoscimento del virus dell’epatite B (per via della unicità dell’eventi di cui si è detto) da parte dell’Organizzazione Mondiale della Sanità, nel 1978, dovendosi fare riferimento alla conoscenza oggettiva ai più alti livelli scientifici, sempre che non emerga altra data antecedente con Io stesso livello di oggettività.»
La Corte di merito, riprendendo in genere la giurisprudenza delle Sezioni Unite in materia (richiamando in particolare Sez. Un. n. 581 del 2008) e, soprattutto, una successiva decisione della terza sezione civile (Cass. n. 17685 del 2011), sostiene che il comportamento omissivo dei controlli da parte dell’Amministrazione ridonda in responsabilità, anche per trattamenti del 1970, precedenti alla data della sicura di conoscenza del’epatite B (1978), in quanto a partire dalla fine degli anni sessanta – inizi anni settanta – era noto il rischio collegato alla trasmissione dell’epatite e Il Ministero della salute è obbligato da una pluralità di fonti normative a esercitare una attività di controllo e vigilanza, anche in ordine alla pratica terapeutica della trasfusione del sangue e dell’uso di emoderivati, rispondendo per omessa vigilanza dei danni conseguenti a infezioni da virus contratte da soggetti trasfusi. Dalle fonti normative si evince che, sin dalla fine degli anni Sessanta/inizi anni Settanta, era noto il rischio di trasmissione di epatite virale, essendo possibile la rilevazione indiretta del virus mediante la rilevazione di valori alti di funzionalità epatica (transaminasi). Sin dalla metà degli anni Sessanta erano esclusi dalla possibilità di donare il sangue coloro che avevano valori di funzionalità epatica alterati rispetto ai limiti prescritti. Il Ministero, a conoscenza del fenomeno, ha, con circolari del 1971 e del 1972, disposto la ricerca sistematica dell’antigene Australia, cui successivamente fu dato il nome di antigene di superficie del virus dell’epatite B; dal 1978 ha reso obbligatoria la ricerca della presenza dell’antigene dell’epatite B in ogni singolo campione. Anche prima della legge n. 107 del 1990 il Ministero era tenuto ad attività di controllo, direttiva e vigilanza in materia di sangue umano. L’omissione di tali attività, funzionali alla tutela della salute pubblica, espone il Ministero a responsabilità extracontrattuale quando dalla violazione del dovere di vigilanza derivi la violazione di interessi giuridicamente rilevanti dei cittadini. In caso di concretizzazione del rischio, che la regola violata tende a prevenire, non può prescindersi dal comportamento dovuto e dalla condotta nel singolo caso tenuta e i danni conseguenti a quest’ultima, costituendone il risultato, rendono presuntivamente provato il nesso di causalità. Le Sezioni Unite, nello specificare che il Ministero risponde per il contagio degli altri virus (HIV e HCV) a partire dalla data di conoscenza dell’epatite B (HBC), trattandosi di forme di manifestazione patogena dello stesso evento lesivo dell’integrità fisica da virus veicolato da sangue infetto, non hanno inteso limitare la rilevanza del fenomeno e la relativa responsabilità alla data di conoscenza dell’epatite B; anzi hanno sottolineato che il rischio è antico quanto la necessità delle trasfusioni. Pertanto, il Ministero non può non ritenersi tenuto, anche anteriormente al 1978, a controllare che il sangue per le trasfusioni o per gli emoderivati fosse esente dai virus de quibus e che i donatori non presentassero alterazioni delle transaminasi. Le Sezioni Unite del 2008 non hanno affrontato espressamente la tematica della responsabilità del Ministero per il periodo precedente al 1978, anno in cui l’Organizzazione mondiale della sanità l’ha ufficialmente riconosciuto. Tuttavia, il principio applicabile emerge chiaramente da quelli, affermati e applicati, in riferimento ai contagi successivi. Emerge, in particolare, dai principi applicati in tema di nesso di causa; ed è proprio su tale snodo cruciale che la decisione della sezione semplice, richiamata dalla Corte di merito, si discosta dalle Sezioni Unite.
Infatti, non sono in discussione gli obblighi del Ministero, derivanti da norme primarie e regolamentari, di direttiva, di vigilanza e di controllo, in materia di impiego di sangue umano per uso terapeutico, finalizzati alla esclusione di rischi di malattie, fattisi più stringenti agli inizi degli anni Settanta in concomitanza al diffondersi delle ricerche scientifiche.
Senza qui ripercorrere i principi applicabili in generale – enucleati con chiarezza dalle Sezioni Unite – è sufficiente sottolineare che il problema della conoscenza del virus è inquadrato nell’ambito della c.d. causalità adeguata o regolarità causale. E, quindi, dando rilievo, per pervenire a una causalità giuridicamente rilevante all’interno delle serie causali determinate ai sensi degli artt. 40 e 41 c.p., solo a quelle cause che, nel momento in cui si produce l’evento causante non appaiono del tutto inverosimili, ma che si presentino come effetto non del tutto imprevedibile, secondo il principio della regolarità causale. Con la conseguenza, che ciascuno è responsabile soltanto delle conseguenze della sua condotta, attiva o omissiva, che appaiono sufficientemente prevedibili al momento nel quale ha agito, escludendosi in tal modo la responsabilità per tutte le conseguenze assolutamente atipiche o imprevedibili. Prevedibilità effettuata con giudizio ex ante e obiettiva, individuata in astratto e non in concreto, non con il metro di valutazione della conoscenza dell’uomo medio, ma delle migliori conoscenze scientifiche del momento, proprio perché si tratta di accertare il nesso causale e non l’elemento soggettivo. Divenendo così rilevante, non la prevedibilità da parte dell’agente, ma la prevedibilità secondo le regole scientifiche. La responsabilità per omissione, inserita entro tale ambito di regolarità causale, e pacificamente accertarle attraverso un giudizio ipotetico, comporta che, individuato preliminarmente l’obbligo di tenere una condotta omessa in capo al soggetto, sussiste il nesso di causa se, secondo un giudizio ipotetico, l’azione omessa avrebbe impedito l’evento, non potendosi riconoscere responsabilità per omissione quando il comportamento omesso, anche se fosse stato tenuto, non avrebbe impedito l’evento; non essendo in tal caso causa del danno lamentato.
5. Condivisibilità della sentenza della Cass. SE. Civ. 6 ordinanza n. 2232 del 2016 nel provvedimento giudiziale del Tribunale di Catanzaro n. 1580/2017
La Cass. Sez. Civ. 6 Ordinanza n. 2232/2016 ha statuito che in caso di patologie conseguenti a infezioni da HCV contratte a seguito di emotrasfusioni non sussistono manifestazioni autonome e diverse ma solo manifestazioni patogene dello stesso elemento lesivo, sicché anche prima del 1978 in cui il virus fu identificato in sede scientifica la responsabilità è del Ministero per i danni da omessa vigilanza in materia di raccolta e distribuzione del sangue. Da queste considerazioni concettuali, statuite dalla Cass. Sez. Civ. 6 Ordinanza n. 2232/2016 il Tribunale Civile di Catanzaro in composizione monocratica con sentenza n. 1580/2017 depositata il 13.10.12017 nel giudizio 4337/2014 Rg. NR. patrocinato a mezzo del difensore avv. Beatrice Biamonte, ha tratto e condiviso il principio, secondo cui: «Premesso che sul Ministero gravava un obbligo di controllo, di direttive e di vigilanza in materia di impiego di sangue umano per uso terapeutico (emotrasfusioni o preparazione di emoderivati), anche strumentale alle funzioni di programmazione e coordinamento in materia sanitaria, affinché fosse utilizzato sangue non infetto e proveniente da donatori conformi agli standard di esclusione di rischi già dal 1970, il giudice, accertata l’omissione di tali attività, accertata, altresì, con riferimento all’epoca di produzione del preparato, la conoscenza oggettiva ai più alti livelli scientifici della possibile veicolazione di virus attraverso sangue infetto e accertata – infine – l’esistenza di una patologia da virus HCV in capo all’attore quale soggetto emotrasfuso o assuntore di emoderivati, ha declarato, in assenza di altri fattori alternativi, che tale omissione sia stata causa dell’insorgenza della malattia, e che, per converso, la condotta doverosa del Ministero, se fosse stata tenuta, avrebbe impedito la versificazione dell’evento» a partire dalla data del suo verificarsi 1974 – proprio per via della raggiunta conoscenza ai più alti livello scientifici della veicolazione del virus. La piena condivisione di tale orientamento da parte del Tribunale di Catanzaro ha quindi escluso che tale principio affermato possa essere limitato esclusivamente alle fattispecie rilevanti, relative a condotte successive al 1978 estendendolo senza dubbio anche ai casi verificatisi tra il 1970 e 1974 come nella fattispecie.
6. Nesso causale
Il Tribunale di Catanzaro ha ritenuto sussistente il nesso di causa fra le trasfusioni praticate al paziente nel 1974 e l’insorgenza di epatite C.
Osserva infatti che l’anamnesi (remota e prossima) del paziente, leggibile nella cartella clinica del ricovero de quo agitur non riporta alcun evento, né patologie o sintomatologie rilevanti ai fini del decidere, e tali da lasciar supporre che l’infezione da virus HCV fosse stata già contratta in data antecedente; piuttosto, la medesima cartella clinica da un lato attesta che il personale sanitario effettivamente praticava due emotrasfusioni, ossia ponendo in essere un intervento astrattamente idoneo a produrre il danno (da contagio) che è motivo della lite, dall’altro non documenta né dimostra che il sangue utilizzato avesse ricevuto una qualsiasi analisi preventiva (ché nulla si legge in proposito, neppure altrove).
Proprio la mancanza di fattori alternativi idonei a produrre l’evento di danno fanno ritenere secondo il Tribunale presuntivamente dimostrato il nesso di causalità tra il contagio da virus HCV, la cui presenza sarebbe stata riscontrata solo diversi anni dopo, e le emotrasfusioni subìte nel 1974.
La sentenza in commento applica dunque il principio di cui alla sentenza n. 582/2008 SS.UU., la quale ha stabilito che la prova del nesso causale, che grava sull’attore danneggiato, tra la specifica trasfusione e il contagio da virus HCV, ove risulti provata l’idoneità di tale condotta a provocarla, può essere fornita anche con il ricorso alle presunzioni (art. 2729 cod. civ.), allorché la prova non possa essere data per non avere la struttura sanitaria predisposto, o in ogni caso prodotto, la documentazione obbligatoria sulla tracciabilità del sangue trasfuso al singolo paziente, e cioè per un comportamento ascrivibile alla stessa parte contro la quale il fatto da provare avrebbe potuto essere invocato.
Il Tribunale di Catanzaro pone inoltre l’accento sul fatto che anche la CTU medico legale disposta in corso di causa aveva riconosciuto la causalità materiale fra trasfusioni di sangue infetto e in favore di soggetti danneggiati da complicanze irreversibili a causa di vaccinazioni obbligatorie, trasfusioni di sangue e somministrazione di emoderivati, costituisce, nel giudizio risarcitorio, «un elemento presuntivo sulla sussistenza del nesso causale tra le trasfusioni e la patologia sicché il giudice che intenda disattenderlo ha l’obbligo di indicare nella motivazione le ragioni di tale scelta» (Cass. n. 6843 del 20/03/2018).
7. Responsabilità del Ministero della Salute
Nel caso in esame il Tribunale di Catanzaro ha ravvisato la responsabilità del Ministero della Salute, in ragione delle competenze attribuitegli dalla legge in materia di vigilanza sanitaria e di uso di sangue umano a scopo terapeutico.
Infatti, anche il consulente tecnico d’ufficio, nella fattispecie, ha ritenuto, sulla base dei documenti prodotti in giudizio e da lui esaminati, che è necessario sottolineare il comportamento omissivo di detto Ministero (id est della Salute) che, oltre all’emanazione di direttive e autorizzazioni in materia di raccolta e lavorazione del sangue umano ed emoderivati, aveva l’obbligo istituzionale di sorveglianza.
Dunque la responsabilità del Ministero convenuto trova la sua fonte sia nel generale precetto dell’articolo 2043 c.c., sia nelle disposizioni che, all’epoca dei fatti (1974), gravavano il Ministero “della Sanità” dell’obbligo di vigilanza in materia sanitaria (dovere da ultimo ribadito con la legge 3 agosto 2001 n. 317, art. 11), nonché del dovere di adottare i provvedimenti indispensabili a evitare che la salute dei cittadini fosse esposta a rischio, per via dell’impiego di sangue umano a uso terapeutico.
8. Quantificazione dei danni
La sentenza n. 1580/2017, dopo aver precisato che la categoria generale del danno non patrimoniale – che attiene alla lesione di interessi inerenti alla persona non connotati da valore di scambio – presenta natura composita, articolandosi in una serie di aspetti (o voci) aventi funzione meramente descrittiva, quali il danno morale (identificabile nel patema d’animo o sofferenza interiore subìti dalla vittima dell’illecito, ovvero nella lesione arrecata alla dignità o integrità morale, quale massima espressione della dignità umana), quello biologico (inteso come lesione del bene salute) e quello esistenziale (costituito dallo sconvolgimento delle abitudini di vita del soggetto danneggiato), dei quali – ove essi ricorrano cumulativamente – occorre tenere conto in sede di liquidazione del danno, in ossequio al principio dell’integralità del risarcimento, ha liquidato i danni sulla base della quantificazione del CTU che ha riconosciuto una invalidità permanente del 5% in capo al ricorrente.
Tale provvedimento è divenuto esecutivo e avverso lo stesso mai è stata proposta alcuna forma di impugnazione. A esso ha fatto seguito il giudizio di ottemperanza al Tar patrocinato a mezzo dello stesso difensore avv. Beatrice Biamonte conclusosi con provvedimento del Tar n. 415/2020 depositato il 06.03.2020 con nomina del Commissario ad acta a fini del ristoro dei danni patiti in favore dell’attore.
avv. Beatrice Biamonte





